
Desde que una compañía comienza a investigar en una molécula innovadora hasta su comercialización (hasta que el medicamento llega al mercado) transcurren entre 10 y 12 años.
En 2022, se invirtieron 304 millones de euros entre las fases de investigación básica, galénica y preclínica.
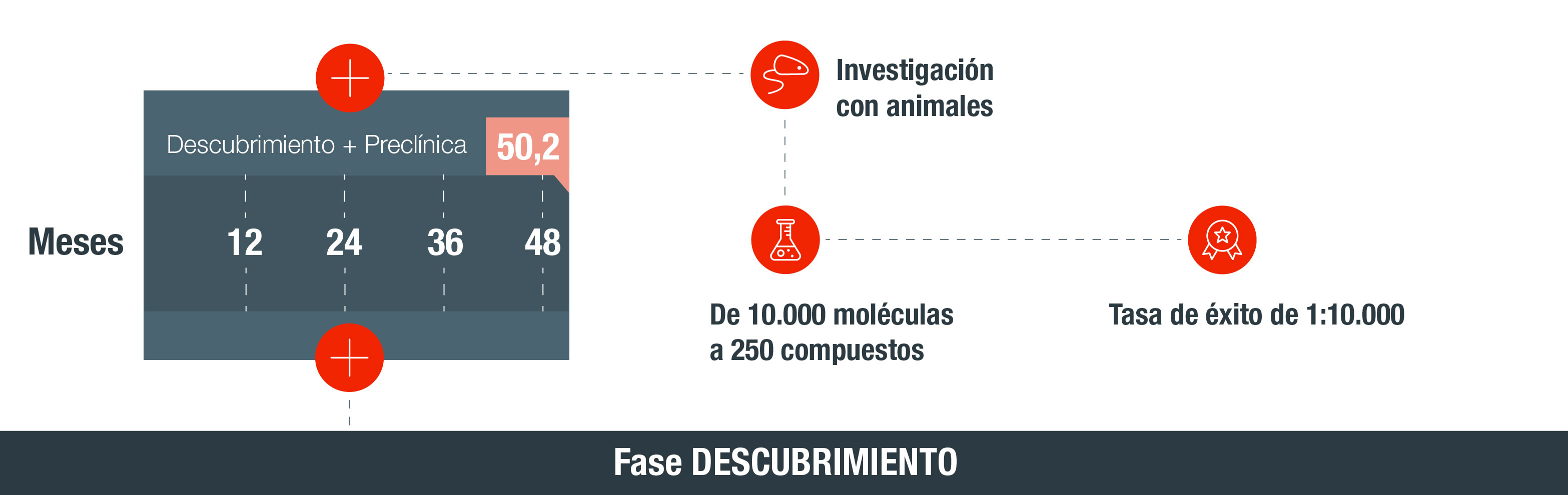
Ver infografía "Cómo se investiga un medicamento"
Identificación de la diana terapéutica. Sustancias químicas asociadas a células o genes que pueden ser el origen de una enfermedad. Se procede a la identificación de las mismas y a la comprensión de cómo funcionan e influyen en una enfermedad específica.
Validación de la diana. Consiste en definir con una mayor exactitud cuál es la relación entre la diana seleccionada y la enfermedad de interés, esto es, el impacto cuantitativo que tiene sobre el proceso patológico la activación o desactivación de la diana en concreto. Se refina la identificación de compuestos que tienen un efecto sobre la diana seleccionada.
Identificación del compuesto líder. Puede ser una estructura química, un compuesto natural, un péptido o un anticuerpo que se une a la diana y tiene un efecto activador o inhibidor sobre ella. Este líder es el punto de partida para desarrollar masivamente moléculas relacionadas, hasta la obtención de una serie de candidatos sobre los que se trabaja en las fases preclínicas.
Validación del compuesto líder. Se comparan varios compuestos líderes y se obtiene información para seleccionar el compuesto o compuestos con mayor potencial para convertirse en un medicamento seguro y efectivo. Generalmente, los estudios de validación incluyen ensayos tanto in vitro como in vivo sobre animales durante los que se comparan distintos compuestos líderes.
En esta fase del desarrollo de un nuevo fármaco, el compuesto seleccionado se ensaya extensivamente en el laboratorio para confirmar que será seguro en su administración en humanos. Esta fase incluye:
Iniciativa dedicada a impulsar la investigación biomédica en España a través de la colaboración de pequeñas empresas biotecnológicas y equipos de investigación con compañías farmacéuticas, que ha atraído desde 2011 un total de 913 proyectos de investigación biomédica. El objetivo esencial es acelerar la transferencia de nuevos medicamentos de pequeñas compañías biotech a la práctica médica.
Farma-Biotech busca el intercambio eficiente de información y el conocimiento personal entre los distintos actores que integran el proceso de investigación y desarrollo de nuevos medicamentos.
Más de catorce años después, se puede afirmar que la iniciativa ha sido un éxito. Farma-Biotech ha analizado desde 2011 más de 900 proyectos de investigación biomédica, de los cuales se han seleccionado un total de 154 proyectos. Han intervenido en las jornadas 59 empresas y 42 centros de investigación y hospitales, presentando los proyectos de investigación avanzada seleccionados por su potencial de innovación, así como 48 compañías farmacéuticas diferentes. En total, más de un centenar de agentes del sector público y privado.